[2026.05.09] 면허는 줬는데, 도로에선 속도제한? 다품목 등재관리의 불편한 진실
2026년 건강보험 약가 개편안에 새롭게 도입된 ‘다품목 등재관리’ 제도. 제네릭 난립을 막겠다는 명분이지만, 정당하게 개발한 제약사에게 예측 불가한 집단 페널티를 안기는 구조적 모순을 담고 있다.
[01] 다품목 등재관리, 쉽게 말하면 무엇인가?
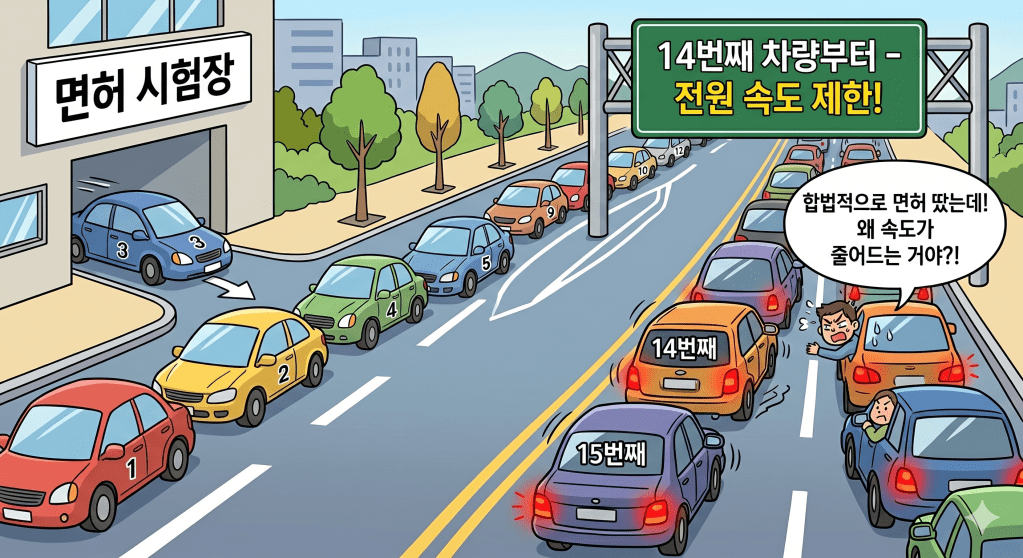
비유를 들어보자. 운전면허를 정상적으로 취득하고 도로에 진입했다. 그런데 같은 도로에 차량이 14대를 넘어서는 순간, 교통당국이 선언한다. “이 도로 혼잡하니 전 차량 속도 제한.” 내가 언제 들어왔든, 얼마나 안전하게 운전하든 상관없다. 그냥 차가 많다는 이유만으로 모두에게 페널티가 주어진다.
다품목 등재관리가 바로 이런 구조다. 오리지널 의약품을 포함해 동일 성분 제품이 건강보험에 14개 이상 등재되는 시점이 되면, 해당 품목군 전체가 ‘다품목 유발 품목’으로 지정된다. 처음 1년은 기존 약가를 유지하지만, 1년이 지나면 자동으로 15%가 인하된다. 아무런 심사 없이, 기계적으로.
생동성시험을 완료한 일반 제네릭: 45% → 1년 후 38.25%
생동성시험 미완료 제네릭: 36% → 1년 후 30.6%
[02] 왜 제약사는 이 상황을 통제할 수 없나?
블록버스터 의약품의 특허가 만료되면 시장에는 신호탄이 쏘아진다. 제약사들은 앞다투어 제네릭을 개발하고, 동시에 20~30개 이상의 품목이 등재 신청을 한다. SGLT-2 계열 당뇨 치료제인 다파글리플로진(dapagliflozin)이나 엠파글리플로진(empagliflozin)이 특허 만료될 때 실제로 벌어진 일이다.
이 상황에서 어느 한 제약사가 “14번째가 되면 약가가 깎이니 나는 진입하지 않겠다”고 결정할 수 있을까? 경쟁사들이 모두 진입하는데 혼자 포기하는 건 시장에서 스스로 퇴장하는 것이나 다름없다. 이른바 ‘죄수의 딜레마’다. 결과적으로 대형 품목에서는 다품목 지정이 사실상 자동으로 발동된다.
핵심은 이것이다. 14번째 등재를 촉발하는 것은 내 의사결정이 아니라 시장 전체의 움직임이다. 즉, 내가 통제할 수 없는 타인의 행동이 나의 약가를 결정하는 구조다.
[03] 그렇다면 제네릭의 실제 약가는 얼마인가?
제도상 제네릭의 등재 약가는 오리지널 대비 45%다. 하지만 대형 품목에서는 등재와 동시에 다품목 지정이 사실상 확정되므로, 1년의 유예기간이 지나면 38.25%로 내려간다. 이것이 항구적인 약가가 된다.
명목 등재 약가 45% → 실질 약가 38.25% (다품목 지정 시, 1년 후 자동 적용)
생동성시험을 완료하지 않은 경우는 더 가혹하다. 이미 45%의 80%인 36%에서 시작해, 1년 후에는 30.6%까지 떨어진다. 제네릭 사업의 손익분기점 자체가 흔들리는 수준이다.
결론은 단순하다. 대형 품목 제네릭의 실제 약가는 45%가 아니라 38.25%다. 그리고 제약사는 등재 시점에 이 사실을 정확히 예측하기 어렵다.
[04] 이 제도의 본질적 모순: 허가는 주고, 약가는 깎는다
제도의 취지는 이해할 수 있다. 동일 성분 제네릭이 수십 개씩 등재되는 현실은 건강보험 재정 관리 측면에서 비효율적이다. 그 수를 줄이고 싶다는 정책 의도는 납득 가능하다.
그런데 수단이 잘못됐다. 진입을 억제하려면 진입 전 단계, 즉 허가 단계에서 막았어야 했다. 하지만 현행 제도는 허가는 정상적으로 내준다. 개발비를 쏟아붓고, 생동성시험을 마치고, 허가를 취득한 기업에게, 건강보험 등재 이후에 예측하지 못한 약가 인하를 부과한다.
허가를 정상적으로 취득한 기업이, 타사의 등재 숫자로 인해, 자신의 약가가 사후적으로 결정되는 구조. 이것은 연대 책임이자 집단 페널티다.
품질이나 혁신성을 기준으로 약가를 차등한 것이 아니다. 단순히 시장에 몇 번째로 들어왔느냐는 순서, 혹은 동시 진입자가 몇 명이냐는 숫자가 약가를 결정한다. 이는 제도 설계의 근본적 오류다.
[05] 신규 제네릭으로 돈 버는 시대는 끝났다
냉정하게 말하면, 이 제도는 제약사에게 하나의 메시지를 보내고 있다. 대형 블록버스터 특허 만료 시장에서 제네릭으로 수익을 내는 전통적인 사업 모델은 더 이상 작동하지 않는다는 것이다.
1+3 자료허여 제도에서 오리지널이 3개 이상의 자료허여를 해주지 않는 것은 당연한 전략이 됐다. 자체 개발을 해서 허가를 받더라도, 대형 품목에서는 다품목 지정을 피할 수 없다. 어느 경로로 진입하든 결과는 같다.
그렇다면 제약사는 무엇을 해야 하는가. 첫째, 38.25%를 실질 약가로 인정하고 사업성을 냉정하게 재평가해야 한다. 45%를 기준으로 세운 사업계획은 이제 유효하지 않다. 둘째, 이미 등재된 기존 제네릭 포트폴리오의 매출 극대화에 집중하는 전략이 신규 진입보다 효율적일 수 있다. 셋째, 제네릭이 아닌 개량신약과 복합제 개발로의 전략적 피벗을 진지하게 검토해야 한다. 혁신형 제약사 인증을 통해 가산 구조에 편입되는 것도 중장기적 선택지다.
마치며…
다품목 등재관리는 제네릭 시장의 구조조정을 시장의 논리가 아닌 정책이 강제하는 제도다. 취지는 이해하더라도 설계는 재검토가 필요하다. 정당하게 개발하고, 정상적으로 허가받은 기업이 예측 불가한 집단 페널티를 받는 구조는 장기적으로 국내 제약 산업의 혁신 동력을 갉아먹을 수 있다. 버틸 것인가, 피벗할 것인가. 지금은 전략적 선택의 시간이다.
Copyright [2026] MarketAccessNow. All rights reserved.

Leave a comment